Проводящие металлы. Удельная электрическая проводимость
Длина и расстояние Масса Меры объема сыпучих продуктов и продуктов питания Площадь Объем и единицы измерения в кулинарных рецептах Температура Давление, механическое напряжение, модуль Юнга Энергия и работа Мощность Сила Время Линейная скорость Плоский угол Тепловая эффективность и топливная экономичность Числа Единицы измерения количества информации Курсы валют Размеры женской одежды и обуви Размеры мужской одежды и обуви Угловая скорость и частота вращения Ускорение Угловое ускорение Плотность Удельный объем Момент инерции Момент силы Вращающий момент Удельная теплота сгорания (по массе) Плотность энергии и удельная теплота сгорания топлива (по объему) Разность температур Коэффициент теплового расширения Термическое сопротивление Удельная теплопроводность Удельная теплоёмкость Энергетическая экспозиция, мощность теплового излучения Плотность теплового потока Коэффициент теплоотдачи Объёмный расход Массовый расход Молярный расход Плотность потока массы Молярная концентрация Массовая концентрация в растворе Динамическая (абсолютная) вязкость Кинематическая вязкость Поверхностное натяжение Паропроницаемость Паропроницаемость, скорость переноса пара Уровень звука Чувствительность микрофонов Уровень звукового давления (SPL) Яркость Сила света Освещённость Разрешение в компьютерной графике Частота и длина волны Оптическая сила в диоптриях и фокусное расстояние Оптическая сила в диоптриях и увеличение линзы (×) Электрический заряд Линейная плотность заряда Поверхностная плотность заряда Объемная плотность заряда Электрический ток Линейная плотность тока Поверхностная плотность тока Напряжённость электрического поля Электростатический потенциал и напряжение Электрическое сопротивление Удельное электрическое сопротивление Электрическая проводимость Удельная электрическая проводимость Электрическая емкость Индуктивность Американский калибр проводов Уровни в dBm (дБм или дБмВт), dBV (дБВ), ваттах и др. единицах Магнитодвижущая сила Напряженность магнитного поля Магнитный поток Магнитная индукция Мощность поглощенной дозы ионизирующего излучения Радиоактивность. Радиоактивный распад Радиация. Экспозиционная доза Радиация. Поглощённая доза Десятичные приставки Передача данных Типографика и обработка изображений Единицы измерения объема лесоматериалов Вычисление молярной массы Периодическая система химических элементов Д. И. Менделеева
Электрические поля регистрируются с использованием системы электрически чувствительных органов в коже. Каждый флакон содержит трубку, заполненную желатиновым веществом, которое контактирует с внешней средой через поры в коже животных. Внутренний конец трубки заканчивается в подвале, где размещаются клетки, которые несут электрические сигналы в нервную систему рыбы. До сих пор ученые не могли объяснить, как слабый электрический сигнал проходит через трубу снаружи в подвал.
Однако теперь физики и биофизика из Калифорнийского университета в Санта-Крус пришли вместе с другими коллегами, что желе является исключительно хорошим протонным проводником, что также объясняется передачей электрических сигналов. Команда попыталась проверить образцы акулы и редиса. Ученые из Розола помещают между двумя палладиевыми электродами, способными поглощать и излучать большое количество протонов. Напряжение, прикладываемое к электродам, заставляет протоны от положительного электрода поступать в желе и двигаться к отрицательному электроду.
Исходная величина
Преобразованная величина
сименс на метр пикосименс на метр мо на метр мо на сантиметр абмо на метр абмо на сантиметр статмо на метр статмо на сантиметр сименс на сантиметр миллисименс на метр миллисименс на сантиметр микросименс на метр микросименс на сантиметр условная единица электропроводности условный коэффициент электропроводности миллионных долей, коэф. пересчета 700 миллионных долей, коэф. пересчета 500 миллионных долей, коэф. пересчета 640 TDS, миллионных долей, коэф. пересчета 640 TDS, миллионных долей, коэф. пересчета 550 TDS, миллионных долей, коэф. пересчета 500 TDS, миллионных долей, коэф. пересчета 700
Протонный ток легко измеряется, потому что он такой же, как электрический ток, протекающий через приложенное напряжение. Хотя измерения показали, что желе является хорошим протонным проводником, он не обеспечивает точное значение проводимости. Протоны должны преодолевать контактное сопротивление, когда они входят и выходят из палладиевых электродов, а измерение проводимости влияет на них. Это было обойдено тем фактом, что измерение проводилось также на двух золотых электродах, помещенных в желе между палладиевыми электродами.
Измерение напряжения между золотыми электродами и током между палладиевыми электродами позволило вычислить точное значение проводимости. Ученые убеждены, что высокая протонная проводимость этого биологического материала связана с наличием цепной молекулы, называемой кератансульфатом. Это кислота, которая означает, что каждая молекула кератинового сульфата может обеспечить протон для повышения проводимости. Эти протоны затем могут перемещаться вдоль цепочек молекул воды, которые образуются вокруг кератансульфата.
Подробнее об удельной электрической проводимости
Введение и определения
Удельная электрическая проводимость (или удельная электропроводность) является мерой способности вещества проводить электрический ток или перемещать электрические заряды в нем. Это отношение плотности тока к напряженности электрического поля. Если рассмотреть куб из проводящего материала со стороной 1 метр, то удельная проводимость будет равна электрической проводимости, измеренной между двумя противоположными сторонами этого куба.
Эксперты считают это открытие очень захватывающим и стимулирующим. Полученные данные должны вдохновлять на дальнейшие исследования функций электрической чувствительности не только ампулы Лоренцини, но и в целом различных органов. Такие данные обычно недоступны. Не только это открытие должно привести к разработке новых типов датчиков разных типов.
Вещества с одинаковой температурой кажутся по-разному теплыми. Если мы коснемся дерева и металла при той же температуре, металл будет выглядеть холодным, потому что это делает наше тепло более теплым и теплым, потому что наша поверхность нагревается нашей рукой.
Удельная проводимость связана с проводимостью следующей формулой:
G = σ(A/l)
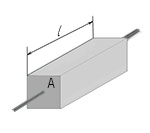
где G - электрическая проводимость, σ - удельная электрическая проводимость, А - поперечное сечение проводника, перпендикулярное направлению электрического тока и l - длина проводника. Эту формулу можно использовать с любым проводником в форме цилиндра или призмы. Отметим, что эту формулу можно использовать и для прямоугольного параллелепипеда, потому что он является частным случаем призмы, основанием которой является прямоугольник. Напомним, что удельная электрическая проводимость - величина, обратная удельному электрическому сопротивлению.
Теплопроводность - это способность материала нагреваться. Фактически это скорость, с которой тепло распространяется от одной нагретой части ткани к другой, холоднее. Теплопроводность каждого вещества определяется коэффициентом теплопроводности. В зависимости от значения коэффициента теплопроводности мы различаем хорошие и плохие теплопроводности.
Все металлы обладают лучшей теплопроводностью. Лучшее тепловыделение приводит к чистым металлам, чем загрязненные металлом или сплавы. Металл, который является лучшим электрическим проводником, также является лучшим проводником тепла. Соотношение между коэффициентом теплопроводности и коэффициентом проводимости выражается в законе Лоренца-Лоренца. Тепловая и электропроводность металлов опосредованы свободными электронами. Хорошая теплопроводность металлов используется в технике, металлических радиаторах, стенках парового котла, охлаждающих телах и т.д. другими твердыми веществами являются плохие теплопроводники, за исключением твердых веществ.
Людям, далеким от физики и техники, бывает сложно понять разницу между проводимостью проводника и удельной проводимостью вещества. Между тем, конечно, это разные физические величины. Проводимость - это свойство данного проводника или устройства (например, резистора или гальванической ванны), в то время как удельная проводимость - это неотъемлемое свойство материала, из которого изготовлены этот проводник или устройство. Например, удельная проводимость меди всегда одинаковая, независимо от того как изменяется форма и размеры предмета из меди. В то же время, проводимость медного провода зависит от его длины, диаметра, массы, формы и некоторых других факторов. Конечно, похожие объекты из материалов с более высокой удельной проводимостью имеют более высокую проводимость (хотя и не всегда).
Опыт практики: очень плохие теплопроводники - это газы и жидкости, особенно вода. При нагревании воды в верхней части трубки мы можем довести ее до кипения, а на дне осталось холодно. Наименьшие коэффициенты теплопроводности имеют газы. Следовательно, также рыхлые пористые вещества, внутри которых находится воздух, являются плохими тепловыми проводниками. Проводимость таких веществ зависит от влажности, так что теплопроводность влажных веществ значительно больше. Вещества, которые являются плохими проводниками тепла, используются для теплоизоляции.

В Международной системе единиц (СИ) единицей удельной электрической проводимости является сименс на метр (См/м) . Входящая в нее единица проводимости названа в честь немецкого ученого, изобретателя, предпринимателя Вернера фон Сименса (1816–1892 гг.). Основанная им в 1847 г. компания Siemens AG (Сименс) является одной из самых больших компаний, выпускающих электротехническое, электронное, энергетическое, транспортное и медицинское оборудование.
Лучшим тепловым изолятором является вакуум. Теплокровные животные нагревают свое тело, чтобы изолировать свое тело, чтобы поддерживать его температуру с минимальной энергией. Хладнокровные животные, с другой стороны, исцеляют свои тела внешними источниками. Тепловая изоляция может помешать им. Утка или китообразные используют свой подкожный жир для теплоизоляции.
Интеллектуальные материалы для нового века. Общим знаменателем этой Нобелевской премии является работа трех ученых, ведущих к открытию и разработке нового класса веществ - проводящих полимеров. Проводящие полимеры сочетают электрическое поведение, типичное для полупроводников с свойствами материала, которые облегчают его обработку. Они могут изменять свою структуру, а потому - в зависимости от реакции на окружающую среду - их физические свойства. Вот почему они называются интеллектуальными материалами. «Умный» атрибут преувеличен, но поведение электропроводящих материалов делает его полезным.

Диапазон удельных электрических проводимостей очень широк: от материалов, обладающих высоким удельным сопротивлением, таких как стекло (которое, между прочим, хорошо проводит электрический ток, если его нагреть докрасна) или полиметилметакрилат (органическое стекло) до очень хороших проводников, таких как серебро, медь или золото. Удельная электрическая проводимость определяется количеством зарядов (электронов и ионов), скоростью их движения и количеством энергии, которое они могут переносить. Средними значениями удельной проводимости обладают водные растворы различных веществ, которые используются, например, в гальванических ваннах. Другим примером электролитов со средними значениями удельной проводимости является внутренняя среда организма (кровь, плазма, лимфа и другие жидкости).
Полимеры обычно известны как изоляторы. Они обладают хорошими механическими свойствами и легко обрабатываются. Они используются в качестве изолирующих электрических проводников, тепловых изоляторов или звукопоглощающих слоев. Их преимуществом является также их низкая плотность, и поэтому они все чаще используются в отраслях, где желателен малый вес материала, например, в авиационной технике или в производстве упаковочных материалов. Для многих применений функциональные свойства полимеров могут быть улучшены путем получения композитов, то есть полимеров, содержащих различные наполнители.
Проводимость металлов, полупроводников и диэлектриков подробно обсуждается в следующих статьях Конвертера физических величин сайт: , и Электрическая проводимость . В этой статье мы обсудим подробнее удельную проводимость электролитов, а также методы и простое оборудование для ее измерения.
Удельная электрическая проводимость электролитов и ее измерение

Так, например, сделаны фоточувствительные слои для ксерографий и лазерных принтеров, пьезоэлектрических и пироэлектрических детекторов или фотокопировальных аппаратов. В композитах, содержащих углеродную сажу или порошковый графит, электропроводность была значительно увеличена. Такие материалы подходят, например, для производства легких нефтяных канистр - проводящий композит обеспечивает электростатический заряд, поэтому нет риска воспламенения летучих паров.
В дополнение к проводящим композитам существуют также конъюгированные полимеры, которые могут проявлять свою высокую электропроводность. Это позволяет регулярно вращать одинарные и двойные связи в молекулярной структуре. В дополнение к системе этих связей предпосылкой является наличие подвижных носителей заряда, которые опосредуют конъюгированный транспорт цепи.
Удельная проводимость водных растворов, в которых электрический ток возникает в результате движения заряженных ионов, определяется количеством носителей заряда (концентрацией вещества в растворе), скоростью их движения (подвижность ионов зависит от температуры) и зарядом, которые они несут (определяемой валентностью ионов). Поэтому в большинстве водных растворов повышение концентрации приводит к увеличению числа ионов и, следовательно, к увеличению удельной проводимости. Однако после достижения определенного максимума удельная проводимость раствора может начать уменьшаться при дальнейшем увеличении концентрации раствора. Поэтому растворы с двумя различными концентрациями одной и той же соли могут иметь одинаковую удельную проводимость.
Структурно самым простым конъюгированным полимером является полиацетилен. Основополагающим открытием этих знатоков было выяснить, что когда тонкая полиацетиленовая пленка легирована парами иода, электропроводность пленки увеличивается примерно в миллион раз. Электрон удаляется из полимерной цепи. После переноса электрона из полиацетиленовой цепи в молекулу иода, которая заряжена отрицательно, молекула полиацетилена несет положительный заряд заряда. Существенное различие между легированием неорганических и органических полупроводников заключается в том, что мы можем существенно влиять на электрические свойства материала при следовых концентрациях легирующей примеси, для неорганических веществ нам нужна более высокая концентрация для полимеров.
Температура также влияет на проводимость, так как при повышении температуры ионы движутся быстрее, что приводит к увеличению удельной проводимости. Чистая вода - плохой проводник электричества. Обычная дистиллированная вода, в которой содержится в равновесном состоянии углекислый газ из воздуха и общая минерализация менее 10 мг/л, имеет удельную электрическую проводимость около 20 мСм/см. Удельная проводимость различных растворов приведена ниже в таблице.
Для переноса электрического заряда переполнение носителей между цепями является определяющим фактором. Этот транспорт менее эффективен, чем перенос заряда в металлах, поскольку он сильно зависит от порядка макромолекул. Доказательство состоит в том, что механически ориентированные пленки показывают более высокую электропроводность в направлении удлинения, чем исходные образцы.
Работа трех лауреатов по-прежнему остается вершиной исследований, начавшихся в 1950-х годах. Уже некоторые исследователи начали заниматься переносом электронов в низкомолекулярных веществах и образованием проводящих солей. В 1960-х годах Хидео Акамату и Хиро Инокучи писали монографию «Органический полупроводник», в которой реальные системы показали, что малые молекулы могут создавать проводники и даже сверхпроводники. В поисках подходящих веществ были синтезированы сотни органических материалов с повышенной электропроводностью, но до сих пор было невозможно приготовить подходящий полимер.


Для определения удельной проводимости раствора используется измеритель сопротивления (омметр) или проводимости. Это практически одинаковые устройства, отличающиеся только шкалой. Оба измеряют падение напряжения на участке цепи, по которому протекает электрический ток от батареи прибора. Измеренное значение проводимости вручную или автоматически пересчитывается в удельную проводимость. Это осуществляется с учетом физических характеристик измерительного устройства или датчика. Датчики удельной проводимости устроены просто: это пара (или две пары) электродов, погруженных в электролит. Датчики для измерения удельной проводимости характеризуются постоянной датчика удельной проводимости , которая в простейшем случае определяется как отношение расстояния между электродами D к площади (электрода), перпендикулярной течению тока А
Анилин черный известен с века. Из-за трудностей в синтезе внимание стало обращать на простейший модельный полимер - полиацетилен. Он имеет две конформации, транс и цис-форму. Синтез дает их смесь. С точки зрения электропроводности интересна только трансформация, полученная Хидеки Ширакавой в чистом виде полимерной пленки серебра. Это помогло ему по совпадению - он использовал катализатор различного типа для полимеризации, чем обычно, плюс тысячная концентрация.
На другом конце света МакДиармид и его коллега Хегер в то время рассматривали свойства неорганического полимера, состоящего из атомов серы и азота, которые они делали в виде пленки, подобной металлической пленке. О свойствах этого полимера было сообщено Макдиармидом на научной встрече в Токио, где он встретил Ширакаву. Они согласились начать совместную работу в Университете Пенсильвании. Транс-полиацетилен засевался иодом и изучал его электропроводность.
Эта формула хорошо работает, если площадь электродов значительно больше расстояния между ними, так как в этом случае большая часть электрического тока протекает между электродами. Пример: для 1 кубического сантиметра жидкости K = D/A = 1 см/1 см² = 1 см⁻¹. Отметим, что датчики удельной проводимости с маленькими электродами, раздвинутыми на относительно большое расстояние, характеризуются значениями постоянной датчика 1.0 cm⁻¹ и выше. В то же время, датчики с относительно большими электродами, расположенными близко друг к другу, имеют постоянную 0,1 cm⁻¹ или менее. Постоянная датчика для измерения удельной электрической проводимости различных устройств находится в пределах от 0,01 до 100 cm⁻¹.
Результатом стал ряд рабочих мест и компаний, которые затем улучшили химические процессы и повысили электропроводность. Хотя полиацетилен обладает высокой проводимостью, приближаясь к проводимости металлов, он не подходит для более широкого использования, он обладает низкой устойчивостью к атмосферным воздействиям. Поэтому интерес исследователей с середины 80-х годов был сфокусирован на других конъюгированных полимерах - полипирроле, политиофене, полианилина, полифенилена, поли.
Полянилин, вероятно, самый старый органический полимер, созданный человеком. Фриче, который вскоре после получения анилина стремился создать новые синтетические красители. Лэтби описал электрохимическое окисление анилина, которое после проталкивания щелочи изменило цвет на синий.

Теоретическая постоянная датчика: слева - K = 0,01 см⁻¹ , справа - K = 1 см⁻¹
Для получения удельной проводимости из измеренной проводимости используется следующая формула:
σ = K ∙ G
σ - удельная проводимость раствора в См/см;
K - постоянная датчика в см⁻¹;
G - проводимость датчика в сименсах.
Постоянную датчика обычно не рассчитывают по его геометрическим размерам, а измеряют в конкретном измерительном устройстве или в конкретной измерительной установке с использованием раствора с известной проводимостью. Эта измеренная величина и вводится в прибор для измерения удельной проводимости, который автоматически рассчитывает удельную проводимость по измеренным значениям проводимости или сопротивления раствора. В связи с тем, что удельная проводимость зависит от температуры раствора, устройства для ее измерения часто содержат датчик температуры, который измеряет температуру и обеспечивает автоматическую температурную компенсацию измерений, то есть, приведение результатов к стандартной температуре 25°C.
Самый простой способ измерения проводимости - приложить напряжение к двум плоским электродам, погруженным в раствор, и измерить протекающий ток. Этот метод называется потенциометрическим. По закону Ома, проводимость G является отношением тока I к напряжению U :
Однако не все так просто, как описано выше - при измерении проводимости имеется много проблем. Если используется постоянный ток, ионы собираются у поверхностей электродов. Также у поверхностей электродов может возникнуть химическая реакция. Это приводит к увеличению поляризационного сопротивления на поверхностях электродов, что, в свою очередь, приводит к получению ошибочных результатов. Если попробовать измерить обычным тестером сопротивление, например, раствора хлористого натрия, будет хорошо видно, как показания на дисплее цифрового прибора довольно быстро изменяются в сторону увеличения сопротивления. Чтобы исключить влияние поляризации, часто используют конструкцию датчика из четырех электродов.
Поляризацию также можно предотвратить или, во всяком случае, уменьшить, если использовать при измерении переменный ток вместо постоянного, да еще и подстраивать частоту в зависимости от проводимости. Низкие частоты используются для измерения низкой удельной проводимости, при которой влияние поляризации невелико. Более высокие частоты используются для измерения высоких проводимостей. Обычно частота подстраивается в процессе измерения автоматически, с учетом полученных значений проводимости раствора. Современные цифровые двухэлектродные измерители проводимости обычно используют переменный ток сложной формы и температурную компенсацию. Они откалиброваны на заводе-изготовителе, однако в процессе эксплуатации часто требуется повторная калибровка, так как постоянная измерительной ячейки (датчика) изменяется со временем. Например, она может измениться при загрязнении датчики или при физико-химических изменениях электродов.
В традиционном двухэлектродном измерителе удельной проводимости (именно такой мы будем использовать в нашем эксперименте) между двумя электродами приложено переменное напряжение и измеряется протекающий между электродами ток. Этот простой метод имеет один недостаток - измеряется не только сопротивление раствора, но и сопротивление, вызванное поляризацией электродов. Для сведения влияния поляризации к минимуму используют четырехэлектродную конструкцию датчика, а также покрытие электродов платиновой чернью.
Общая минерализация
Устройства для измерения удельной электрической проводимости часто используют для определения общей минерализации или содержания твёрдых веществ (англ. total dissolved solids, TDS). Это мера общего количества органических и неорганических веществ, содержащихся в жидкости в различных формах: ионизированной, молекулярной (растворенной), коллоидной и в виде суспензии (нерастворенной). К растворенным веществам относятся любые неорганические соли. Главным образом, это хлориды, бикарбонаты и сульфаты кальция, калия, магния, натрия, а также некоторые органические вещества, растворенные в воде. Чтобы относиться к общей минерализации, вещества должны быть или растворенными, или в форме очень мелких частиц, которые проходят сквозь фильтры с диаметром пор менее 2 микрометров. Вещества, которые постоянно находятся в растворе во взвешенном состоянии, но не могут пройти сквозь такой фильтр, называется взвешенными твердыми веществами (англ. total suspended solids, TSS). Общее количество взвешенных веществ обычно измеряется для определения качества воды.

Существует два метода измерения содержания твердых веществ: гравиметрический анализ , являющийся наиболее точным методом, и измерение удельной проводимости . Первый метод - самый точный, но требует больших затрат времени и наличия лабораторного оборудования, так как воду нужно выпарить до получения сухого остатка. Обычно это производится при температуре 180°C в лабораторных условиях. После полного испарения остаток взвешивается на точных весах.
Второй метод не такой точный, как гравиметрический анализ. Однако он очень удобен, широко распространен и является наиболее быстрым методом, так как представляет собой простое измерение проводимости и температуры, выполняемое за несколько секунд недорогим измерительным прибором. Метод измерения удельной электропроводности можно использовать в связи с тем, что удельная проводимость воды прямо зависит от количества растворенных в ней ионизированных веществ. Данный метод особенно удобен для контроля качества питьевой воды или оценки общего количества ионов в растворе.
Измеренная проводимость зависит от температуры раствора. То есть, чем выше температура, тем выше проводимость, так как ионы в растворе при повышении температуры движутся быстрее. Для получения измерений, независимых от температуры, используется концепция стандартной (опорной) температуры, к которой приводятся результаты измерения. Опорная температура позволяет сравнить результаты, полученные при разных температурах. Таким образом, измеритель удельной проводимости может измерять реальную проводимость, а затем использовать корректирующую функцию, которая автоматически приведет результат к опорной температуре 20 или 25°C. Если необходима очень высокая точность, образец можно поместить в термостат, затем откалибровать измерительный прибор при той же температуре, которая будет использоваться при измерениях.
Большинство современных измерителей удельной проводимости снабжены встроенным датчиком температуры, который используется как для температурной коррекции, так и для измерения температуры. Самые совершенные приборы способны измерять и отображать измеренные значения в единицах удельной проводимости, удельного сопротивления, солености, общей минерализации и концентрации. Однако еще раз отметим, что все эти приборы измеряют только проводимость (сопротивление) и температуру. Все физические величины, которые показывает дисплей, рассчитываются прибором с учетом измеренной температуры, которая используется для автоматической температурной компенсации и приведения измеренных значений к стандартной температуре.
Эксперимент: измерение общей минерализации и проводимости
В заключение мы выполним несколько экспериментов по измерению удельной проводимости с помощью недорогого измерителя общей минерализации (называемого также солемером, салинометром или кондуктомером) TDS-3. Цена «безымянного» прибора TDS-3 на eBay с учетом доставки на момент написания статьи менее US$3.00. Точно такой же прибор, но с названием изготовителя стоит уже в 10 раз дороже. Но это для любителей платить за брэнд, хотя очень высока вероятность того, что оба прибора будут выпущены на одном и том же заводе. TDS-3 осуществляет температурную компенсацию и для этого снабжен датчиком температуры, расположенным рядом с электродами. Поэтому его можно использовать и в качестве термометра. Следует еще раз отметить, что прибор реально измеряет не саму минерализацию, а сопротивление между двумя проволочными электродами и температуру раствора. Все остальное он автоматически рассчитывает с использованием калибровочных коэффициентов.

Измеритель общей минерализации поможет определить содержание твердых веществ, например, при контроле качества питьевой воды или определения солености воды в аквариуме или в пресноводном пруде. Его можно также использовать для контроля качества воды в системах фильтрации и очистки воды, чтобы узнать когда пришло время заменить фильтр или мембрану. Прибор откалиброван на заводе-изготовителе с помощью раствора хлорида натрия NaCl с концентрацией 342 ppm (частей на миллион или мг/л). Диапазон измерения прибора - 0–9990 ppm или мг/л. PPM - миллионная доля, безразмерная единица измерения относительных величин, равная 1 10⁻⁶ от базового показателя. Например, массовая концентрация 5 мг/кг = 5 мг в 1 000 000 мг = 5 частей на миллион или миллионных долей. Точно так же, как процент является одной сотой долей, миллионная доля является одной миллионной долей. Проценты и миллионные доли по смыслу очень похожи. Миллионные доли, в отличие от процентов, удобны для указания концентрации очень слабых растворов.
Прибор измеряет электрическую проводимость между двумя электродами (то есть величину, обратную сопротивлению), затем пересчитывает результат в удельную электрическую проводимость (в англоязычной литературе часто используют сокращение EC) по приведенной выше формуле проводимости с учетом постоянной датчика K, затем выполняет еще один пересчет, умножая полученную удельную проводимость на коэффициент пересчета 500. В результате получается значение общей минерализации в миллионных долях (ppm). Подробнее об этом - ниже.
Данный прибор для измерения общей минерализации нельзя использовать для проверки качества воды с высоким содержанием солей. Примерами веществ с высоким содержанием солей являются некоторые пищевые продукты (обычный суп с нормальным содержанием соли 10 г/л) и морская вода. Максимальная концентрация хлорида натрия, которую может измерить этот прибор - 9990 ppm или около 10 г/л. Это обычная концентрация соли в пищевых продуктах. Данным прибором также нельзя измерить соленость морской воды, так как она обычно равна 35 г/л или 35000 ppm, что намного выше, чем прибор способен измерить. При попытке измерить такую высокую концентрацию прибор выведет сообщение об ошибке Err.
Солемер TDS-3 измеряет удельную проводимость и для калибровки и пересчета в концентрацию использует так называемую «шкалу 500» (или «шкалу NaCl»). Это означает, что для получения концентрации в миллионных долях значение удельной проводимости в мСм/см умножается на 500. То есть, например, 1,0 мСм/см умножается на 500 и получается 500 ppm. В разных отраслях промышленности используют разные шкалы. Например, в гидропонике используют три шкалы: 500, 640 и 700. Разница между ними только в использовании. Шкала 700 основана на измерении концентрации хлорида калия в растворе и пересчет удельной проводимости в концентрацию выполняется так:
1,0 мСм/см x 700 дает 700 ppm
Шкала 640 использует коэффициент преобразования 640 для преобразования мСм в ppm:
1,0 мСм/см x 640 дает 640 ppm
В нашем эксперименте мы вначале измерим общую минерализацию дистиллированной воды. Солемер показывает 0 ppm. Мультиметр показывает сопротивление 1,21 МОм.

Для эксперимента приготовим раствор хлорида натрия NaCl с концентрацией 1000 ppm и измерим концентрацию с помощью TDS-3. Для приготовления 100 мл раствора нам нужно растворить 100 мг хлорида натрия и долить дистиллированной воды до 100 мл. Взвесим 100 мг хлорида натрия и поместим его в мерный цилиндр, добавим немного дистиллированной воды и размешаем до полного растворения соли. Затем дольем воду до метки 100 мл и еще раз как следует размешаем.
Для экспериментального определения проводимости мы использовали два электрода, изготовленные из того же материала и с теми же размерами, что и электроды TDS-3. Измеренное сопротивление составило 2,5 КОм.
Теперь, когда нам известно сопротивление и концентрация хлорида натрия в миллионных долях, мы можем приблизительно рассчитать постоянную измерительной ячейки солемера TDS-3 по приведенной выше формуле:
K = σ/G = 2 мСм/см x 2,5 кОм = 5 см⁻¹
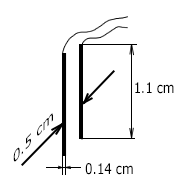
Это значение 5 см⁻¹ близко к расчетной величине постоянной измерительной ячейки TDS-3 с указанными ниже размерами электродов (см. рисунок).
- D = 0,5 см - расстояние между электродами;
- W = 0,14 см - ширина электродов
- L = 1,1 см - длина электродов
Постоянная датчика TDS-3 равна K = D/A = 0,5/0,14x1,1 = 3,25 cm⁻¹. Это не сильно отличается от полученного выше значения. Напомним, что приведенная выше формула позволяет лишь приблизительно оценить постоянную датчика.
Вы затрудняетесь в переводе единицы измерения с одного языка на другой? Коллеги готовы вам помочь. Опубликуйте вопрос в TCTerms и в течение нескольких минут вы получите ответ.
Из курса физики Вы помните, что электрическое сопротивление любого проводника может быть рассчитано по формуле:
где R - сопротивление в Ом;
l - длина проводника, см;
S - площадь поперечного сечения, см 2 ;
r - удельное сопротивление, т.е. сопротивление проводника длиной 1 см с площадью поперечного сечения 1 см 2 .
В электрохимии принято пользоваться величинами, обратными указанным:
Величина L называется электрической проводимостью и измеряется в Сименсах (См) См = Ом -1 .
Величина À называется удельной электрической проводимостью. Нетрудно вывести, что величина À измеряется в См×см -1 . На рис.3.1. представлена кондуктометрическая ячейка, применяемая для измерения электрической проводимости. Она представляет собой сосуд 1, без дна, в который вставлены два платиновых электрода 2, помещаемые в исследуемый раствор 3.
Величину К определяют экспериментально. Для этого необходимо измерить электрическую проводимость L раствора, для которого À известна. Обычно для этого используют растворы хлорида калия известной концентрации (0,1; 0,05; 0,01 моль/дм 3), величины À которых имеются в таблицах.
Из уравнения (3.5.) следует, что
удельная проводимость - это электрическая проводимость раствора, помещенного между двумя электродами площадью 1 см 2 , находящимися на расстоянии 1 см.
| À HCl KOH HF CH 3 COOH С Рис.3.2.Зависимость удельной прово-димости от концентрации | Удельная электрическая проводимость раствора зависит от природы растворителя и растворенного вещества, кон-центрации раствора и темпера-туры. На рис.3.2. приведены графики зависимости À от концентрации водных раство-ров некоторых электролитов при постоянной температу-ре.Из рисунка, прежде всего следует, что при равных концентрациях растворов про-водимость растворов сильных электролитов значительно выше, т.к. в них содержится |
больше ионов-носителей электричества. В разбавленных растворах как сильных так и слабых электролитов увеличение концентрации приводит к повышению проводимости, что связано с увеличением количества ионов. В области высоких концентраций наблюдается уменьшение À. Для сильных электролитов это связано с увеличением вязкости растворов и усилением электростатического взаимодействия между ионами. Для слабых электролитов указанный эффект связан с уменьшением степени диссоциации и, следовательно, уменьшением количества ионов.
При повышении температуры удельная проводимость электролитов увеличивается:
À 2 = À 1 [ 1 + a(T 2 - T 1)] (3.7.)
В этом уравнении À 1 и À 2 – удельная проводимость при температурах Т 1 и Т 2 , а a – температурный коэффициент проводимости. Например, для солей a » 0,02. Это означает, что повышение температуры на один градус приводит к увеличению проводимости приблизительно на 2%. Связано это с тем, что при повышении температуры уменьшается степень гидратации и вязкость растворов.
Следует отметить, что в отличие от электролитов, электричес-кая проводимость металлов при повышении температуры уменьшается.
Молярная электрическая проводимость
Молярная проводимость l связана с удельной проводимостью формулой:
l = À×1000/с (3.8.)
В этом выражении с - молярная концентрация раствора, моль×дм -3 . Молярная проводимость выражена в См×см 2 ×моль -1 . Итак,
молярная проводимость - это проводимость раствора, содержащего 1 моль вещества при расстоянии между электродами, равном 1 см.
Молярная электрическая проводимость как сильных так и слабых электролитов с увеличением концентрации понижается. Характер зависимости l от с для сильных и слабых электролитов различен, т.к. влияние концентрации обусловлено различными причинами.
Сильные электролиты . При небольших концентрациях зависимость молярной проводимости от концентрации выражается эмпирическим уравнением Кольрауша:
l = l 0 –bÖс (3.9.)
где b – определяемая опытным путем постоянная,
а l 0 – молярная электрическая проводимость при бесконечном разбавлении или предельная молярная проводимость .
Таким образом,
liml C ® 0 = l 0 (3.10.)
Приготовить раствор, концентрация которого равна нулю, невозможно. Величину l 0 для сильных электролитов можно определить графически. Из уравнения (3.9.) следует, что график зависимости l = f(Öc) для сильных электролитов представляет собой прямую линию (рис.3.3.,линия 1).
Если приготовить ряд растворов различной концентрации, измерить их проводимость L,рассчитать и построить график l = f(Öс), то экстраполируя полученную прямую на ось ординат (с = 0), можно определить l 0 . Если учесть, что сильные электролиты, независимо от концентрации раствора полностью диссоциированы, то приходим к выводу, что количество ионов, образуемых из 1 моль вещества, всегда одно и то же. Значит, от концентрации раствора зависит скорость движения ионов, с увеличением концентрации усиливается торможение ионов . Это явление, связано с образованием вокруг каждого иона в растворе ионной атмосферы , состоящей преимущественно из ионов противоположного знака. С увеличением концентрации также увеличивается вязкость раствора. Существуют и другие причины замедления движения ионов в электрическом поле, на которых мы останавливаться не будем.
Если экспериментально определить величину l для раствора данной концентрации и графически найти l 0 можно рассчитать величину коэффициента электропроводности f :
f = l / l 0 (3.11.)
Коэффициент f характеризует степень торможения ионов и при разбавлении раствора стремится к единице.
Слабые электролиты . Молярная проводимость слабых электролитов значительно меньше, чем для растворов сильных электролитов (рис.3.3, линия 2). Это связано с тем, что даже при низких концентрациях степень диссоциации слабых электролитов мала. Повышение молярной проводимости слабых электролитов при разбавлении растворов связано с увеличением степени диссоциации в соответствии с законом разбавления Оствальда. С.Аррениус высказал предположение, что молярная проводимость слабого электролита связана с его степенью диссоциации выражением:
a = l / l 0 (3.12.)
Таким образом, степень диссоциации слабого электролита можно рассчитать, если известна его предельная молярная проводимость l 0 . Однако определить l 0 графически путем экстраполяции графика l= f(Öс) нельзя, т.к. кривая (рис.3.3., линия 2) при уменьшении концентрации асимптотически приближается к оси ординат.
Величину l 0 можно определить с помощью закона независимости движения ионов Кольрауша :
Молярная электрическая проводимость электролита при бесконечном разбавлении раствора равна сумме предельных подвижностей катионов и анионов.
l 0 =l 0,+ + l 0,– (3.13.)
Подвижности катиона и аниона пропорциональны абсолютным скоростям движения ионов (см.табл. 3.1.).
l 0,+ = F×U + ; l 0,– = F×U – (3.14.)
В этих формулах F - единица количества электричества, называемая Фарадеем, равная 96494 Кулонов (Кл). В табл.3.2. приведены предельные подвижности некоторых ионов.
Следует отметить, что закон независимости движения ионов справедлив как для слабых, так и для сильных электролитов.
Таблица 3.2.
Предельные подвижности ионов (см 2 ×См×моль -1) при 25 0 С
| Катион | l 0,+ | Анион | l 0,– |
| Н + К + Na + Li + Ag + Ba 2+ Ca 2+ Mg 2+ | 349,8 73,5 50,1 38,7 61,9 127,2 119,0 106,1 | ОН - I - Br - Cl - NO 3 - CH 3 COO - SO 4 2- | 76,8 78,4 76,3 71,4 40,9 160,0 |
Применение измерений проводимости
Метод исследования основанный на измерении электрической проводимости, называется кондуктометрией . Этот метод широко используется в лабораторной практике. Прибор для измерения электрической проводимости называется кондуктометром . В частности, кондуктометрический метод позволяет определять константы диссоциации слабых электролитов.
Пример. Определение константы диссоциации уксусной кислоты.
а)Для нахождения постоянной кондуктометрической ячейки приготовили растворы хлорида калия с молярными концентрациями 0,1 и 0,02 моль×дм -3 и измерили их проводимость.Она оказалась равной соответственно L 1 = 0,307 См и L 2 = 0,0645 См. По таблице находим значения удельной проводимости растворов хлорида калия указанных концентраций:
À 1 = 1,29×10 -1 См×см -1 ; À 2 = 2,58×10 -2 См×см -1
По уравнению 3.6. рассчитываем постоянную ячейки:
К 1 = À 1 /L 1 = 0,42 см -1
К 2 = À 2 /L 2 = 0,40 см -1
Среднее значение К = 0,41 см -1
б)Приготовили два раствора уксусной кислоты с концентрациями c 1 =0,02моль×дм -3 и c 2 = 1×10 -3 моль×дм -3 . С помощью кондуктометра измерили их электрическую проводимость:
L 1 = 5,8×10 -4 См; L 2 = 1,3×10 -4 См.
в) Рассчитываем удельную проводимость:
À 1 = L 1 ×K = 5,8×10 -4 ×0,41 = 2,378×10 -4 Cм×см -1
À 2 = L 2 ×К = 1,2×10 -4 ×0,41 = 0,492×10 -4 См×см -1
г) По формуле (3.8.) находим молярную электрическую проводимость l 1 =11,89См×см 2 ×моль -1 ; l 2 = 49,2 См×см 2 ×моль -1
д) Находим, пользуясь табл.3.2. величину предельной молярной прово-димости уксусной кислоты: l 0 = 349,8 +40,9 = 390,7 См×см 2 ×моль -1 .
е) Наконец, рассчитываем для каждого раствора степень диссоциации (уравнение 3.12.) и константу диссоциации
a 1 = 3,04×10 -2 ; a 2 = 1,26×10 -1
К 1 = 1,91×10 -5 ; К 2 = 1,82×10 -5
Среднее значение К = 1,86×10 -5
